C-C键裂解研究进展,你关注了吗?
时间: 2020-10-19
作者: 百灵威
分享:
C-C键高效选择性裂解在化合物的构建及反应路线的优化中有重要研究意义。然而,与日趋成熟的C-C键形成方法相比,其裂解反应在有机合成中仍具有挑战性,主要源于以下几点:
- C-C键键能较高,反应活性低,难以活化
- C-C键与C-H键存在选择性问题
- 同一分子中不同C-C键也存在选择性问题
醇类化合物通过氧原子与金属配位,经β-碳消除过程可实现醇类化合物α-碳与β-碳的C-C单键活化,是一类有趣的转化。至今为止研究较多的反应过程包括β-炔基消除、β-芳基消除、β-烷基消除。
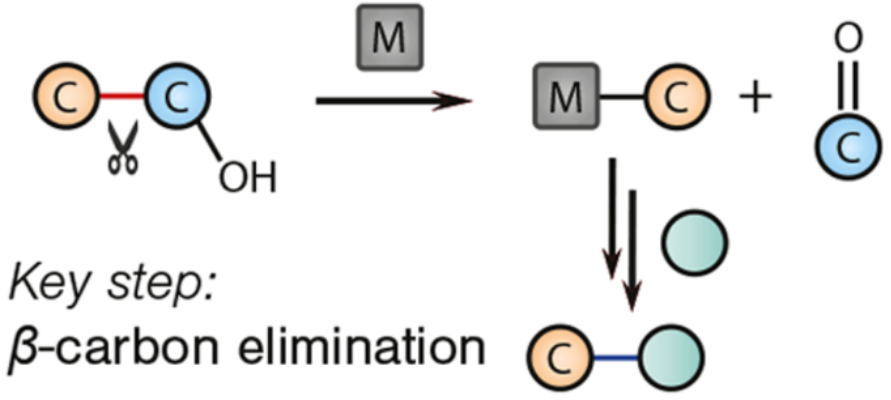
来源:Chemical Reviews
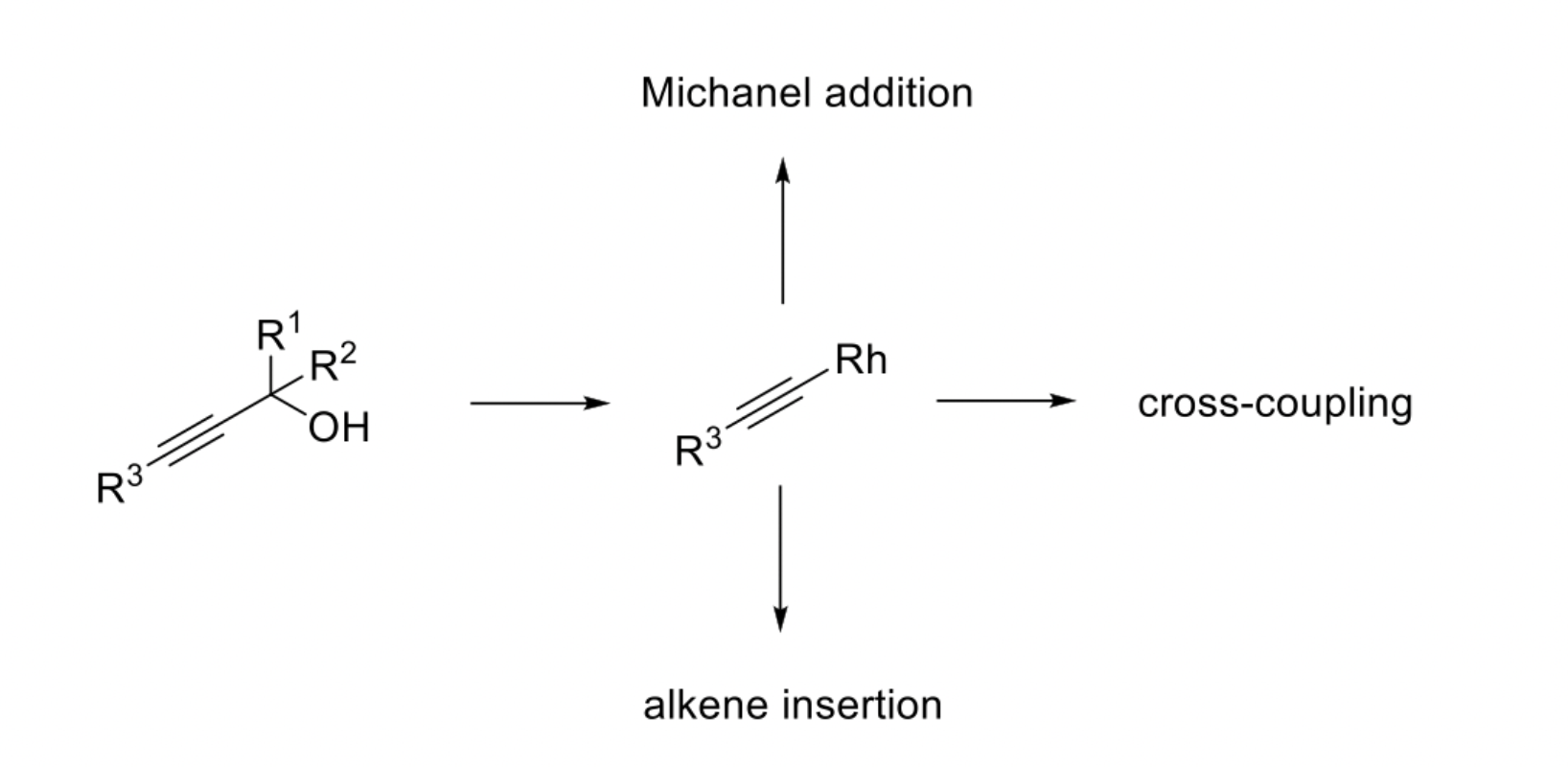
β-炔基消除
这类反应过程研究较多的金属为铑(Rh)。醇类化合物经上述过程可生成炔基-Rh物种,随后可参与炔烃插入或Michanel加成反应。此外,炔基-Rh物种也可通过传统氧化加成、还原消除等偶联过程得到芳基炔化合物。
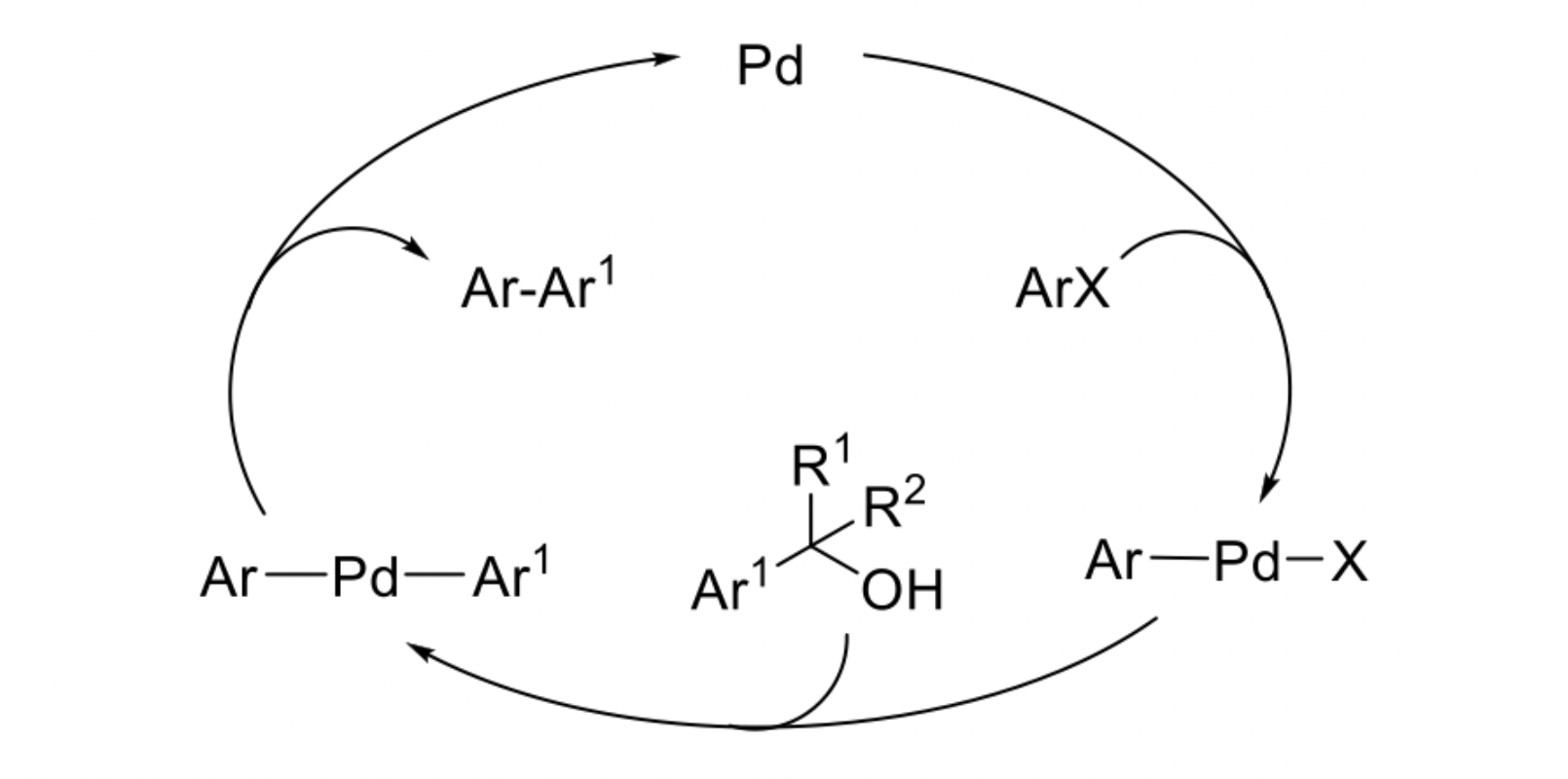
β-芳基消除
这类反应过程研究较多的金属为钯(Pd)。三级醇类化合物一般经β-碳消除过程,原位生成芳基亲核试剂参与Pd催化的传统偶联反应,反应温度一般较高。
β-烷基消除
这类过程研究较少,且需要配位基团辅助反应进行(如吡啶、氧化吡啶、羰基、呋喃等)。
- C(sp3)−C(sp3)键裂解局限于特殊的骨架
- 二级及一级醇的C-C活化
此外,苛刻的反应条件制约反应进一步应用,发展温和的条件(如自由基介导的C-C活化)是下一步研究方向。
参考文献
- Lutz, M. D., & Morandi, B. (2020). Metal-Catalyzed Carbon–Carbon Bond Cleavage of Unstrained Alcohols. Chemical Reviews.