N-苯基唑基膦配体的不对称C-H官能化
时间: 2023-09-18
作者: 百灵威
分享:
β2-和β3-氨基酸是合成天然产物中药物和拟肽的重要手性成分。
特别是,将β-氨基酸掺入肽中可以调节其二级结构并提高其蛋白水解稳定性,从而为肽模拟物提供了更高的药理学价值[1]。
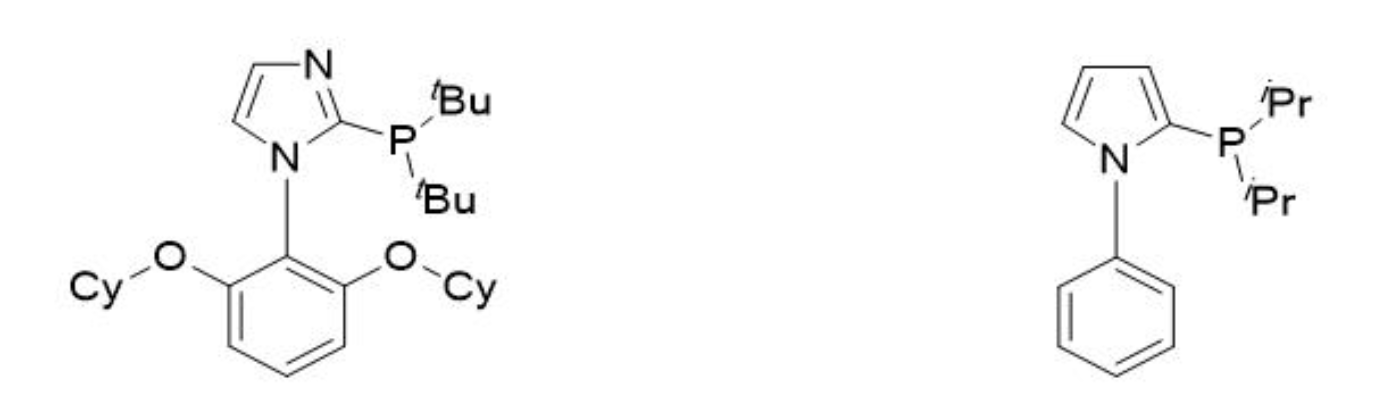
图1.N-苯基唑基膦配体
在早期的报道中,带有咪唑(15-3360)或吡咯(15-3365)环的N-苯基唑的膦配体(图1),在钯催化配体控制的无环N-Boc胺的α-和β-芳基化反应中[2]。
和在烯基三氟甲磺酸酯和壬酯与带有芳基的仲烷基溴化物进行Barbier Negishi偶联反应中显示出有效的性能[3]。
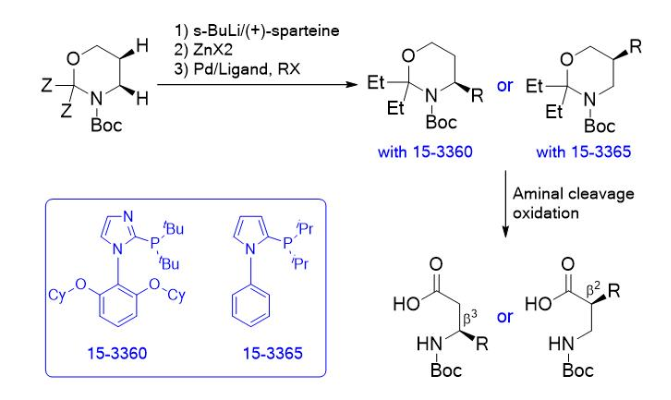
图2.N-苯基唑基膦配体
根岸偶联反应的区域选择性是高度配体控制的,并且能够仅获得C4或C5官能化产物。该反应在大量的实例中均展现出高的对应选择性,且使用(+)-天冬氨酸替代物开发了手性二胺的催化形式。随后,根据锂化步骤中使用的天冬氨酸对映体,将选定的C4和C5官能化的Boc-1,3-恶嗪转化为具有(R)或(S)构型的高度对映体富集的β2-和β3-氨基酸。
参考文献
1. Nat. Catal. 2019, 2, 882.
2. Angew. Chem. Int. Ed. 2014, 53, 2678.
3. Angew. Chem. Int. Ed. 2018, 57, 1982.
![2-[Bis(1-methylethyl)phosphino]-1-phenyl-1H-pyrrole, min. 95%; 2- [双(1-甲基乙基)膦基] -1-苯基-1H-吡咯, 95% , min.95%](https://www.jkchemical.com/static/Structure/918/9188193.png)
![1-[2,6-Bis(cyclohexyloxy)phenyl]-2-(di-tertbutylphosphaneyl)-1H-imidazole, min. 95%; 1- [2,6-双(环己氧基)苯基] -2-(二叔丁基膦酰基)-1H-咪唑,95% , min. 95%](https://www.jkchemical.com/static/Structure/918/9188192.png)